Фуллерены
Каркас молекулы С60 состоит из 12 правильных пятиугольников (пентагонов) и 20 немного искаженных шестиугольников (гексагонов). Диаметр молекулы составляет 0.71 нм. Группа симметрии икосаэдра состоит из 120 элементов симметрии, включая 6 осей симметрии пятого порядка (через центры пентагонов), 10 осей третьего порядка (через центры гексагонов) и 15 осей второго порядка (перпендикулярно ребру между гексагонами). В икосаэдрической структуре молекулы С60 все атомы углерода эквивалентны, каждый атом принадлежит двум шестиугольникам и одному пятиугольнику и связан с ближайшими соседями двойной и двумя одиночными ковалентными связями. Непланарность молекул приводит к сильным напряжениям, вследствие чего фуллерены термодинамически менее стабильны, чем графит. Энергия напряжения забирает 80 % теплоты формирования.
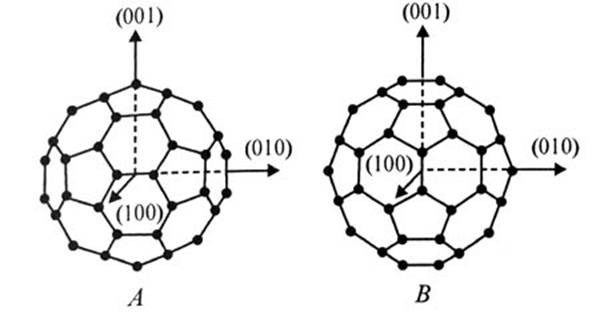
Рисунок1. Молекула фуллерена С60 в стандартных ориентациях А и В
относительно кристаллографических осей.
Для рассмотрения вопроса о длине связей в молекуле фуллерена вспомним понятие гибридизации атомных орбит. Электронная оболочка атома углерода содержит четыре валентных электрона конфигурации s^2p^2. Валентные электроны атома находятся на разных орбитах, отличающихся друг от друга распределением электронного облака в пространстве. На основании этого можно было бы предположить наличие связей, не равноценных ни по направлению, ни по прочности: p-орбиты должны создавать более прочные связи, чем s-орбиты. Однако, по данным, например, рентгеноструктурного анализа, молекула ВСl3(хлорид бора) содержит совершенно эквивалентные связи. Для объяснения подобных фактов было предположено, что валентные электроны формируют связи не за счет чистых s,p,d,f-орбит, а за счет смешанных, гибридных орбит. При гибридизации обеспечивается гораздо большее перекрытие электронных облаков вдоль линии, соединяющей центры атомов, чем в случае негибридизированных волновых функций. Благодаря этому происходит понижение энергии всей молекулы и упрочнение связей. При sp^3-гибридизации углам между направлениями, вдоль которых гибридные волновые функции имеют максимумы, соответствуют тетраэдрические значения 109°28'. Гибридизация d^2sp^3 дает октаэдр. В конфигурации алмаза каждый из четырех валентных электронов углерода принадлежит тетрагонально направленной sp^3-гибридной орбитали, которая создает прочную сигма-связь с соседним атомом. В случае графита каждый из трех валентных электронов принадлежит тригонально направленной sp2-гибридной орбитали, участвующей в формировании сильных внутреслойных сигма-связей, а четвертый электрон находится на орбитали pп, направленной перпендикулярно сигма-плоскости. Эта орбиталь формирует слабые, делокализованные пи-связи со своими соседями, при этом пи-связь часто называют ненасыщенной связью. Для графита расстояние между атомами в узлах гексагональной сетки равно 0.142 нм, а между сетками (слоями) 0.335 нм. Для простоты принято говорить, что углеродные атомы фуллереновой клетки имеют sp^2-гибридизацию. Однако это не совсем так, поскольку это возможно только для планарных структур, а отклонение приводит к частичной регибридизации. Для С60 примешивание сигма-связей приводит к состоянию sp^2. Связи, которыми соединяются 2 гексагона ((6,6)-связь, 0.139 нм), двойные и они короче, чем одиночные связи на границе пентагона и гексагона ((5,6)-связь, 0.145 нм). Различия в длине связей ослабевают для С60^-6 и исчезают для С60^-12. Для К6С60 длины связей равны 0.142 и 0.145 нм, в то время как для Li12С60 (6,6)-связь становится длиннее (5,6)-связи: 0.145 и 0.144 нм. Следовательно, причина чередования связей — в заселенности молекулярных орбиталей.
3. Электронная структура С60
Диаграмма энергетических уровней изолированной молекулы С60 схематически показана на рисунке 2. Колебательные состояния, связанные с каждым электронным состоянием, лежат выше
соответствующего бесколебательного уровня на энергию (E), равную целому числу квантов энергии колебаний. Поглощение и испускание света между основным состоянием и первым возбужденным синглетным состоянием должны отсутствовать из-за того, что такие переходы запрещены по соображениям симметрии. Поэтому оптические переходы между этими состояниями могут происходить только при участии фононов.
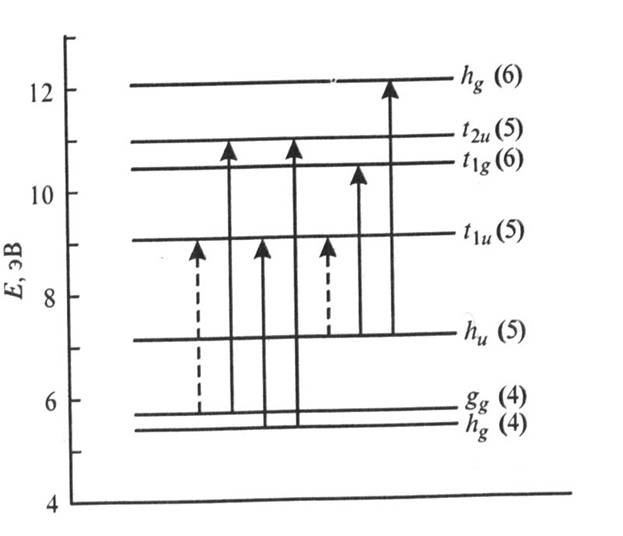
Рисунок 2. Диаграмма энергетических уровней изолированной молекулы С60.
Экспериментальные и теоретические работы свидетельствовали о том, что энергия электронных переходов между наивысшей заполненной и наинизшей незаполненной молекулярными
орбиталями (HOMO—LUMO) в С60 (как в изолированной молекуле, так и в конденсированном состоянии) лежит в оптическом диапазоне. Первое детальное теоретическое исследование электронной структуры С60 в твердотельном состоянии было выполнено Саито и Ошиямой. Физические свойства молекулы определяются ее электронной структурой, и в этом отношении С60 не имеет аналогов. В молекуле С60 имеется 60 пи-электронов, которые находятся в наименее связанных состояниях и, таким образом, определяют, как С60 будет связываться с другими атомами или молекулами в твердом состоянии.
Распределение по энергиям этих пи-электронов показано на рис. 3. Пары пи-электронов с противоположным спином заполняют 30 нижних энергетических состояний (эти уровни показаны на рисунке 3). Обозначения уровней a, t, g и h соответствуют кратностям вырождения 1, 3, 4 и 5, а индексы g и и относятся к четной и нечетной симметрии волновой функции. Число состояний на уровне определяется побочным квантовым числом L; самый нижний уровень ag (L = 0) содержит одно состояние, следующий t1u (L = 1) содержит три состояния и т.д. Уровень с моментом L = 5, содержащим 11 состояний, на которых могут разместиться 22 электрона, вследствие икосаэдрической симметрии оказывается расщеплен на три отдельных уровня: hu + t1u + t2u. На самом нижнем из них, hu, находится 10 электронов, и это есть наивысшая заполненная молекулярная орбиталь; следующий уровень, t1u, называется наинизшей незаполненной молекулярной орбиталью, на нем может располагаться до 6 электронов.
Перейти на страницу: 1 2 3 4 5 6 7 8 9 10
