Кристаллы в природе
Объяснения заключается в особенности строения молекул, из которых состоят эти вещества. Молекулы холестерика - почти такие же, как в нематической жидкости, но имеют на своём конце небольшой отросток (рис57а). Этот отросток образуется обычно одним или несколькими атомами, которые выступают из основной плоскости, содержащей подавляющее большинство атомов молекулы. Симметрия молекулы нарушается из-за отростка и напоминает симметрию руки, которая бывает только правой и только левой.
Как сказывается такая форма молекул на ориентационном порядке жидкости? Подобные молекулы можно расположить параллельно друг другу в определённой плоскости, например в плоскости, в которойлежат сами молекулы. Именно эти плоскости и образуют отдельные слои холестерика (рис57б). А как могут быть «пристроены» друг к другу эти слои? Очевидно, что молекулы слоя 2 могут быть параллельны молекулам слоя 1, если слои расположены друг от друга на расстоянии, примерно равном высоте отростков. В этом случае отростки не мешают молекулам оставаться параллельными.
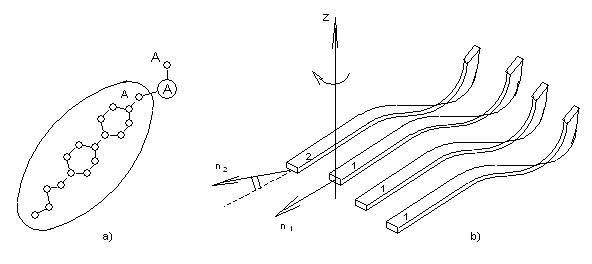
рис. 57
Если расстояние между слоями меньше высоты отростков, то векторы n1 и n2 не могут быть строго параллельны – мешают отростки. Поэтому между векторами n1 и n2 имеется малый угол α.
Таким образом, мы приходим к выводу, что несимметричные молекулы должны образовывать стопку нематических слоёв, причём от слоя к слою молекулы должны поворачиваться на определённый угол α. В зависимости от того, как изогнуты отростки отдельных молекул, холестерические спирали могут быть либо правыми, либо левыми.
7.3.Жидкие кристаллы-растворы.
Жидкокристаллическое состояние можно получить и при растворении подходящих веществ в растворителе, например в воде, который сам по себе не образует жидкий кристалл. При этом получается самые разные жидкие кристаллы. Если молекулы растворяемого вещества имеют форму стержня – получается нематическая жидкость; если у стержнеобразных молекул имеются отростки - холестерическая жидкость. Можно получить и более сложные состояния.
В таких жидких кристаллах важную роль играют не только силы притяжения между молекулами, но и силы отталкивания молекул на близких расстояниях. Роль сил отталкивания можно наглядно представить себе следующим образом. В большом объёме при высокой температуре молекулы, например стержнеобразные, не подчиняются никакому ориентационному порядку, то есть поворачиваются в пространстве как угодно. Но чтобы при всевозможных поворотах молекулы не мешали друг другу, надо каждой молекуле отвести в жидкости определённый объём. Этот объём представляет собой кубик с размером ребра, примерно равным длине молекулы l; в пределах такого кубика с объёмом l3 молекула действительно может быть ориентирована как угодно.
Поместим теперь тоже число молекул при той же температуре в меньший объём, то есть повысим плотность системы. В результате на каждую молекулу станет приходиться объём, меньший, чем l3. Как будут размещаться молекулы в этом случае? Естественно, они смогут разместиться в меньшем объёме, если не будут поворачиваться как угодно, задевая друг друга, а займут более или менее параллельные положения. Если размер поперечного сечения молекул а заметно меньше l и на каждую молекулу приходится объём ~а2l, то все молекулы должны быть ориентированы одинаково, так как только в этом случае они не задевают друг друга. Но это может лишь произойти в случае очень высокой плотности. При средней плотности, когда на каждую молекулу приходится объём, меньший, чем l3, но больший чем а2l, ориентационный порядок будет неполным, но заметным. И связан этот порядок с тем, что молекулы не могут из-за сильного отталкивания проникать друг в друга.
Плотность стержнеобразных молекул можно изменять без заметного изменения общего объёма жидкости, когда такие молекулы растворяются в каком-нибудь обычном растворителе, например в воде. Повышая содержание воды в соответствующем растворе, мы получаем обычную неориентированную жидкость. При очень малом же содержании растворителя образуется нематическая или холестерическая жидкость, в зависимости от деталей структуры молекул. Растворы полимерных молекул являются как раз нематическими жидкими кристаллами.
Работу клеток живого организма во многом определяют жидкие кристаллы-растворы, которые образуются из специальных молекул. Эти молекулы устроены более сложно. Их взаимодействие друг с другом и с молекулами растворителя характеризуются силами отталкивания и силами электростатического притяжения. Она состоит из небольшой головки (рис58а), представляющей собой электрический диполь, и длинного незаряжённого хвоста.
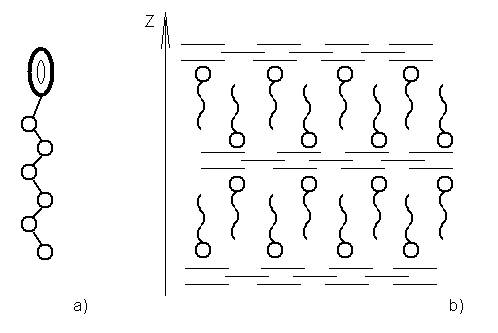
рис.58
Напомним, что молекулы воды - тоже электрические диполи. Противоположно заряжённые концы диполей притягиваются друг к другу, и поэтому молекулярные головки притягивают воду. В тоже время хвосты молекул химически устроены так, что они отталкивают воду, как молекулы жиров или воска.
7.4. Смектическая жидкость.
Строение особых молекул, описанных выше, объясняет большое разнообразие структуры жидких кристаллов-растворов. Например, при определённой концентрации таких молекул в воде могут получаться жидкие кристаллы, в которых молекулы не только одинаково ориентируется, но и образуют жесткую кристаллическую решетку. Только эта решетка лишь отчасти похожа на обычную решётку твёрдого тела, периодическую в трёх взаимно перпендикулярных направлениях. Таких направлений в особых жидких кристаллах может быть только два или даже одно.
На рисунке 58,б изображена стопка слоёв, образующихся при не очень малой концентрации молекул в воде. Хвосты молекул как бы «прячутся» от воды за оболочками из дипольных головок. Вода является прослойкой между двойными слоями молекул. Стопка таких слоёв образует кристаллическую решётку, периодическую только в одном направлении - вдоль оси Z. В этом направлении жесткость решётки почти такая же, как в твёрдом теле, в то время как в поперечных направлениях слои могут свободно скользить, то есть вдоль слоёв система ведёт себя как жидкость. Такая структура сродни мылу, поэтому такие жидкие кристаллы называются смектическими. Они похожи на холестерики своей слоистостью, но периоды решёток в этих двух случаях различны. В холестериках период составляет несколько тысяч ангстрем, а в смектиках - несколько десятков ангстрем (что соответствует длине молекулы).
Перейти на страницу: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29
