Свойства жидкостей
Строение жидкостей
Жидкое состояние, занимая промежуточное положение между газами и кристаллами, сочетает в себе некоторые черты обоих этих состояний. В частности, для жидкостей, как и для кристаллических тел, характерно наличие определённого объёма, и вместе с тем жидкость, подобно газу, принимает форму того сосуда, в котором она находиться, но в отличие от газов не занимает весь объём сосуда. Каждая молекула жидкости, также как и в твердом теле, «зажата» со всех сторон соседними молекулами и совершает тепловые колебания около некоторого положения равновесия. Однако, время от времени любая молекула может переместиться в соседнее вакантное место. Такие перескоки в жидкостях происходят довольно часто; поэтому молекулы не привязаны к определенным центрам, как в кристаллах и могут перемещаться по всему объему жидкости. Этим объясняется текучесть жидкостей. Согласно рентгенографическим исследованиям, в отношении характера расположения частиц жидкости занимают промежуточное состояние. В расположении частиц жидкости наблюдается так называемый ближний порядок (рис. 1).
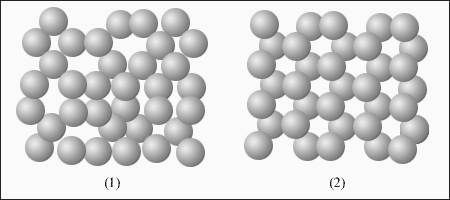
Рис 1.
Пример ближнего порядка молекул жидкости и дальнего порядка молекул кристаллического вещества: 1 – вода; 2 – лед.
Это означает, что по отношению к любой частице расположение ближайших к ней соседей является упорядоченным. Однако по мере удаления от данной частицы расположение по отношению к ней других частиц становиться всё менее упорядоченным, и довольно быстро порядок в расположении частиц полностью исчезает. В кристаллах имеет место дальний порядок: упорядоченное расположение частиц по отношению к любой частице наблюдается в пределах значительного объёма. (рис. 1).
Наличие в жидкостях ближнего порядка служит причиной того, что структуру жидкостей называют квазикристаллической (кристаллоподобной).
Из-за отсутствия дальнего порядка жидкости, за не многими исключениями, не обнаруживают анизотропии, характерной для кристаллов с их правильным расположением частиц. В жидкостях с удлиненными молекулами наблюдается одинаковая ориентация молекул в пределах значительного объёма, чем обуславливается анизотропия оптических и некоторых других свойств. Такие жидкости получили название жидких кристаллов. У них упорядочена только ориентация молекул, взаимное же расположение молекул, как и в обычных жидкостях, дальнего порядка не обнаруживает.
Промежуточным положением обусловлено то обстоятельство, что жидкое состояние оказывается особенно сложным по своим свойствам. Поэтому его теория гораздо менее развита, чем теория кристаллического и газообразного состояний.
Жидкости, как и твердые тела, изменяют свой объем при изменении температуры. Для не очень больших интервалов температур относительное изменение объема ΔV / V0 пропорционально изменению температуры ΔT:
![]()
Коэффициент β называют температурным коэффициентом объемного расширения. Этот коэффициент у жидкостей в десятки раз больше, чем у твердых тел. У воды, например, при температуре 20 °С βв ≈ 2·10–4 К–1, у стали βст ≈ 3,6·10–5 К–1, у кварцевого стекла βкв ≈ 9·10–6 К–1.
Тепловое расширение воды имеет интересную и важную для жизни на Земле аномалию. При температуре ниже 4 °С вода расширяется при понижении температуры (β < 0). Максимум плотности ρв = 103 кг/м3 вода имеет при температуре 4 °С.
При замерзании вода расширяется, поэтому лед остается плавать на поверхности замерзающего водоема. Температура замерзающей воды подо льдом равна 0 °С. В более плотных слоях воды у дна водоема температура оказывается порядка 4 °С. Благодаря этому может существовать жизнь в воде замерзающих водоемов.
Поверхностное натяжение
Наиболее интересной особенностью жидкостей является наличие свободной поверхности. Жидкость, в отличие от газов, не заполняет весь объем сосуда, в который она налита. Между жидкостью и газом (или паром) образуется граница раздела, которая находится в особых условиях по сравнению с остальной массой жидкости. Молекулы в пограничном слое жидкости, в отличие от молекул в ее глубине, окружены другими молекулами той же жидкости не со всех сторон. Силы межмолекулярного взаимодействия, действующие на одну из молекул внутри жидкости со стороны соседних молекул, в среднем взаимно скомпенсированы. Любая молекула в пограничном слое притягивается молекулами, находящимися внутри жидкости (силами, действующими на данную молекулу жидкости со стороны молекул газа (или пара) можно пренебречь). В результате появляется некоторая равнодействующая сила, направленная вглубь жидкости. Если молекула переместиться с поверхности внутрь жидкости, силы межмолекулярного взаимодействия совершат положительную работу. Наоборот, чтобы вытащить некоторое количество молекул из глубины жидкости на поверхность (т. е. увеличить площадь поверхности жидкости), надо затратить положительную работу внешних сил ΔAвнеш, пропорциональную изменению ΔS площади поверхности:
ΔAвнеш = σΔS.
Коэффициент σ называется коэффициентом поверхностного натяжения (σ > 0). Таким образом, коэффициент поверхностного натяжения равен работе, необходимой для увеличения площади поверхности жидкости при постоянной температуре на единицу.
В СИ коэффициент поверхностного натяжения измеряется в джоулях на метр квадратный (Дж/м2) или в ньютонах на метр (1 Н/м = 1 Дж/м2).
Следовательно, молекулы поверхностного слоя жидкости обладают избыточной по сравнению с молекулами внутри жидкости потенциальной энергией. Потенциальная энергия Ep поверхности жидкости пропорциональна ее площади:
Ep = Aвнеш = σS.
Из механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии. Отсюда следует, что свободная поверхность жидкости стремится сократить свою площадь. По этой причине свободная капля жидкости принимает шарообразную форму. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы называются силами поверхностного натяжения.
