Свойства газов
Абсолютная температура
Легко видеть, что давление газа, заключенного в постоянный объем, не является прямо пропорциональным температуре, отсчитанной по Шкале Цельсия. Это ясно, например, из таблицы, приведенной в предыдущей главе. Если при 100° С давление газа равно 1,37 кг1см2, то при 200° С оно равно 1,73 кг/см2. Температура, отсчитанная по термометру Цельсия, увеличилась вдвое, а давление газа увеличилось только в 1,26 раза. Ничего удивительного, конечно, в этом нет, ибо шкала термометра Цельсия установлена условно, без всякой связи с законами расширения газа. Можно, однако, пользуясь газовыми законами, установить такую шкалу температур, что давление газа будет прямо пропорционально температуре, измеренной по этой новой шкале. Нуль в этой новой шкале называют абсолютным нулем. Это название принято потому, что, как было доказано английским физиком Кельвином (Вильямом Томсоном) (1824—1907), ни одно тело не может быть охлаждено ниже этой температуры.
В соответствии с этим и эту новую шкалу называют шкалой абсолютных температур. Таким образом, абсолютный нуль указывает температуру, равную -273° по шкале Цельсия, и представляет собой температуру, ниже которой не может быть ни при каких условиях охлаждено ни одно тело. Температура, выражающаяся цифрой 273°+t1 представляет собой абсолютную температуру тела, имеющего по шкале Цельсия температуру, равнуюt1. Обычно абсолютные температуры обозначают буквой Т. Таким образом, 2730+t1=T1. Шкалу абсолютных температур часто, называют шкалой Кельвина и записывают Т° К. На основании сказанного
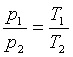 (7)
(7)
Полученный результат можно выразить словами: давление данной массы газа, заключенной в постоянный объем, прямо пропорционально абсолютной температуре. Это — новое выражение закона Шарля.
Формулой (6) удобно пользоваться и в том случае, когда давление при 0°С неизвестно.
Объем газа и абсолютная температура
Из формулы (6), можно получить следующую формулу:
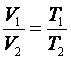 (8)
(8)
- объем некоторой массы газа при постоянном давлении прямо пропорционален абсолютной температуре. Это — новое выражение закона Гей-Люссака.
Зависимость плотности газа от температуры
Что происходит с плотностью некоторой массы газа, если температура повышается, а давление остается неизменным?
Вспомним, что плотность равна массе тела, деленной на объем. Так как масса газа постоянна, то при нагревании плотность газа уменьшается вот столько раз, во сколько увеличился объем.
Как мы знаем, объем газа прямо пропорционален абсолютной температуре, если давление остается постоянным. Следовательно, плотность газа при неизменном давлении обратно пропорциональна абсолютной температуре. Если d1 и d2— плотности газа при температурах t1 и t2 , то имеет место соотношение
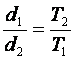 (9)
(9)
Объединенный закон газового состояния
Мы рассматривали случаи, когда одна из трех величин, характеризующих состояние газа (давление, температура и объем), не изменяется. Мы видели, что если температура постоянна, то давление и объем связаны друг с другом законом Бойля— Мариотта; если объем постоянен, то давление и температура связаны законом Шарля; если постоянно давление, то объем и температура связаны законом Гей-Люссака. Установим связь между давлением, объемом и температурой некоторой массы газа, если изменяются все три эти величины.
Пусть начальные объем, давление и абсолютная температура некоторой массы газа равны V1, P1 и Т1, конечные — V2, P2 и T2 - Можно представить себе, что переход от начального к конечному состоянию произошел в два этапа. Пусть, например, сначала изменился объем газа от V1 до V2, причем температура Т1, осталась без изменения. Получившееся при этом давление газа обозначим Pср Затем изменилась температура от Т1 до T2 при постоянном объеме, причем давление изменилось от Pср. до P. Составим таблицу:
Закон Бойля — Мариотта
Р1V1t1
PcpV2T1
Закон Шарля
PcpV2T1
P2V2T2
Пименяя, к первому переходу закон Бойля-Мариотта запишем
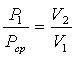 или
или 
Применяя ко второму переходу закон Шарля, можно написать
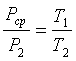
Перемножив эти равенства почленно и сокращая на Pcp получим:
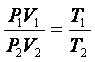 (10)
(10)
Итак, произведение объема некоторой массы, газа на его давление пропорционально абсолютной температуре газа. Это и есть объединенный закон газового состояния или уравнение состояния газа.
Закон Дальтона
До сих пор мы говорили о давлении какого-нибудь одного газа — кислорода, водорода и т. п. Но в природе и в технике мы очень часто имеем дело со смесью нескольких газов. Самый важный пример этого — воздух, являющийся смесью азота, кислорода, аргона, углекислого газа и других газов. От чего зависит давление смеси газов?
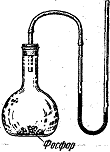
Поместим в колбу кусок вещества, химически связывающего кислород из воздуха (например, фосфор), и быстро закроем колбу пробкой с трубкой. присоединенной к ртутному манометру. Через некоторое время весь кислород воздуха соединится с фосфором. Мы увидим, что манометр покажет меньшее давление, чем до удаления кислорода. Значит, присутствие кислорода в воздухе увеличивает его давление.
Точное исследование давления смеси газов было впервые произведено английским химиком Джоном Дальтоном (1766—1844) в 1809 г. Давление, которое имел бы каждый из газов, составляющих смесь, если бы удалить остальные газы из объема, занимаемого смесью, называют парциальным давлением этого газа. Дальтон нашел, что давление смеси газов равно сумме парциальных давлений их (закон Дальтона). Заметим, что к сильно сжатым газам закон Дальтона неприменим, так же как и закон Бойля — Мариотта.
Перейти на страницу: 1 2 3 4 5 6 7 8
