Изопроцессы в газах
Введение
С помощью уравнения состояния идеального газа можно исследовать процессы, в которых масса газа и один из трех параметров — давление, объем или температура — остаются неизменными. Количественные зависимости между двумя параметрами газа при фиксированном значении третьего параметра называют газовыми законами.
Газ не сохраняют ни форму, ни объем. Характер молекулярного движения в газах – беспорядочное (хаотическое) движение.
Когда в газе происходят какие-либо процессы, то обычно изменяются все три его параметра: p, V, T. Естественно, что наиболее просты такие процессы, которые протекают при изменении только двух параметров, а третий остается постоянным.
Процессы, протекающие при неизменном значении одного из параметров, называют изопроцессами. Правда, в действительности ни один процесс не может протекать при строго фиксированном значении какого-либо параметра. Всегда имеются те или иные воздействия, нарушающие постоянство температуры, давления или объема. Лишь в лабораторных условиях удается поддерживать постоянство того или иного параметра с хорошей точностью, но в действующих технических устройствах и в природе это практически неосуществимо. Изопроцесс - это идеализированная модель реального процесса, которая только приближенно отражает действительность.
Уравнение состояние идеального газа
Состояния данной массы газа характеризуется тремя макроскопическими параметрами: давлением, объемом, температурой. В данной главе рассмотрим между ними связь, а затем посмотрим, для чего эта связь нужна.
Уравнение состояния идеального газа – называется такое уравнение, которое связывает три макроскопических параметра давление P, объем V и температуру T, для достаточно разряженного газа.
Выведем уравнение состояния идеального газа. Для этого подставим в уравнение:
![]() (1)
(1)
выражение для концентрации молекул газа ![]()
![]() , концентрацию газа можно записать так:
, концентрацию газа можно записать так:
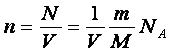 (2)
(2)
где ![]() -постоянная Авогадро, m – масса газа, M – его молярная масса.
-постоянная Авогадро, m – масса газа, M – его молярная масса.
После подстановки (2) в (1) будем иметь
![]()
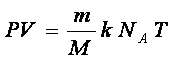 (3)
(3)
где k – постоянная Больцмана. Произведение постоянной Больцмана k и постоянной Авогадро ![]() называется универсальной (молярной) газовой постоянной и обозначается буквой R.
называется универсальной (молярной) газовой постоянной и обозначается буквой R.
![]()
Подставим универсальную газовую постоянную в уравнение (3), получим уравнение состояния для произвольной массы идеального газа:
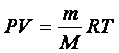 (4)
(4)
Единственная величина в этом уравнении (4), зависящая от рода газа, это его молярная масса.
Уравнение (4) называется уравнение состояния идеального газа или уравнение Менделеева – Клапейрона.
Из уравнения состояния вытекает связь между давлением, объемом и температурой идеального газа, который может находиться в двух любых состояниях.
Если индекс 1 обозначить параметры, относящиеся к первому состоянию, а индекс 2 - параметры, относящиеся ко второму состоянию, то согласно уравнению (4) для газа данной массы:
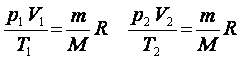
Правые части этих уравнений одинаковы, следовательно, должны быть равны и их левые части:
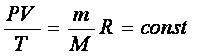 (5)
(5)
Уравнение состояние в форме (5) называется уравнением Клапейрона и представляет собой одну из форм записи уравнения состояния.
Таким образом, для данной массы газа, как бы ни менялись его давление, объем и температура, произведение давления на объем, деленное на абсолютную температуру, есть величина постоянная.
Изотермический процесс
Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называется изотермическим.
Для поддержания температуры газа постоянной необходимо, чтобы он мог обмениваться теплотой с большой системой – термостатом. Термостатом может служить атмосферный воздух, если температура его заметно не меняется на протяжении всего процесса.
Из уравнения состояния идеального газа (4) следует, что при постоянной температуре Т и неизменных значениях массы газа m и его молярной массы M произведение давления Р газа на его объем V должно оставаться постоянным:
PV = const при T = const
Для газа данной массы произведение давления газа на его объем постоянно, если температура газа не меняется.
Изотермический процесс можно осуществить, например, путем изменения объема газа при постоянной температуре.
Этот закон экспериментально был открыт английским ученым Р. Бойлем (1627-1691) и несколько позже французским ученым Э. Мариоттом (1620-1684). Поэтому он носит название закона Бойля – Мариотта.
Закон Бойля – Мариотта справедлив для любых газов, а также и для их смесей (например, для воздуха). Лишь при давлениях, в несколько сотен раз больших атмосферного, отклонения от этого закона становятся существенными.
Зависимость давления газа от объема при постоянной температуре графически изображается кривой, которая называется изотермой. Изотерма газа изображается обратно пропорциональную зависимость между давление и объемом.
